- 技术(专利)类型 实用新型
- 申请号/专利号 201110241744.9
- 技术(专利)名称 一种手性噁唑啉及其合成方法
- 项目单位
- 发明人 罗梅
- 行业类别 人类生活必需品
- 技术成熟度 详情咨询
- 交易价格 ¥面议
- 联系人 罗梅
- 发布时间 2022-07-08
 北京
北京
客服热线:010-83278899
 微信公众号 扫一扫 关注我们
微信公众号 扫一扫 关注我们

项目简介
一种手性噁唑啉,其特征在于:由以下化学式表示的、其化学名称为2-[(4S)-4,5-二氢化-4-R-3-噁唑啉基]苯酚
说明书
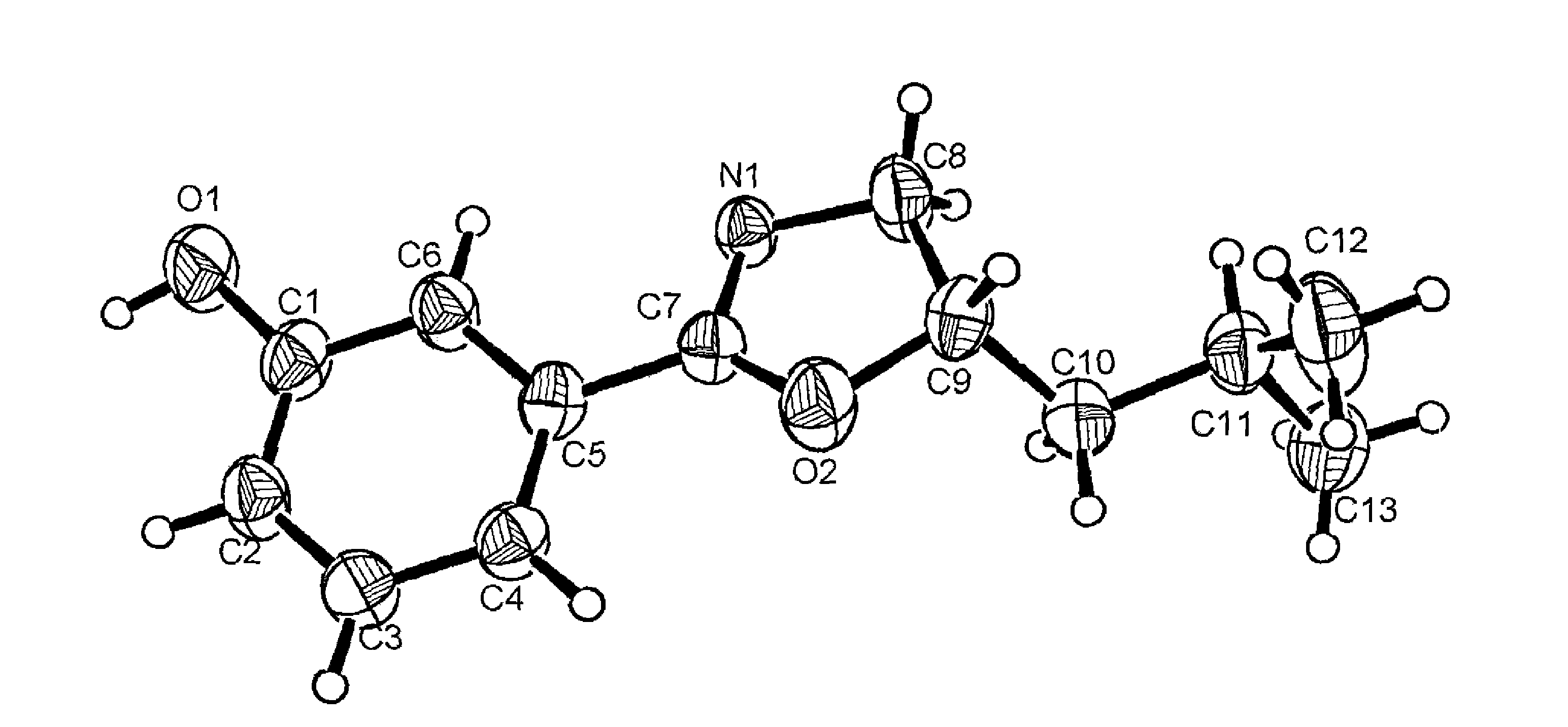
一、技术领域本发明涉及一种新化合物及其制备方法,特别涉及一种手性化合物及其制备方法,确切地说是一种手性噁唑啉及其合成方法。二、背景技术手性噁唑啉及金属配合物在不对称催化领域如Diels-Alder(狄乐-爱而特)二烯环加成反应、Michael(米歇尔)缩合反应、Friedel-Crafts(傅瑞德-克拉佛兹)缩合反应、Aldol(醇醛)缩合反应等许多反应中表现出良好的催化活性和高对映选择性,因而受到广泛的关注。见参考文献【1-2】。2009年,European Journal of Medicinal Chemistry报道了类似化合物的医药用途。见参考文献【3】。参考文献:1.Synthesis of chiral aryloxazoline hydroaluminum and its asymmetric reduction for ketones.Wu,Hai-Chen;Xu,Dong-Cheng;Hua,Wen-Ting.Huaxue Xuebao(2001),59(8),1340-1343.2.Enantioselective addition of diethylzinc to aromatic aldehydes with chiral 2-oxazolinyl phenol as catalysts.Li,Xin-sheng;Wu,Xiao-hua;Fang,Ke-ming.Zhejiang Shifan Daxue Xuebao,Ziran Kexueban(2005),28(4),413-416.3.Chiral 3-(4,5-dihydrooxazol-2-yl)phenyl alkylcarbamates as novel FAAH inhibitors:Insight into FAAH enantioselectivity by molecular docking and interaction fields.Myllymaki,Mikko J.;Kasnanen,Heikki;Kataja,Antti O.;Lahtela-Kakkonen,Maija;Saario,Susanna M.;Poso,Antti;Koskinen,Ari M.P.European Journal of Medicinal Chemistry(2009),44(10),4179-4191.三、发明内容本发明旨在为不对称合成领域特别是制备手性药物提供一种高效的手性催化剂,所要解决的技术问题是遴选相应的原料并建立相应的方法合成手性催化剂。(一)本发明所称的手性噁唑啉是以下化学式所示的化合物: 其化学名称:2-[(4S)-4,5-二氢化-4-R-3-噁唑啉基]苯酚,简称化合物(I)。本手性噁唑啉的合成方法包括合成、分离和纯化,所述的合成就是邻氰基苯酚与手性L-亮氨醇在有机溶剂中有催化剂存在的条件下于110~145℃反应20~30小时,催化剂用量为原料量的50~60wt%(重量百分比,下同)。优选120~140℃反应22~28小时,催化剂用量为原料量的55wt%其化学反应式如下:
所述的有机溶剂选择惰性的、其沸点与反应温度相适应的有机溶剂,比如甲基吡啶或氯苯或二氯苯或乙苯或二甲苯或丙苯或烷烃或卤代烷烃等。这时合成可在回流条件下进行。所述的催化剂选自稀土金属氯化物(三氯稀土)或过渡金属氯化物(ZnCl2、CuCl2、NiCl2、CoCl2、FeCl3、MnCl2等)或AlCl3或烷氧基金属化合物(四异丙氧基钛、二甲基二氯锡烷等)。优选三氯稀土或过渡金属氯化物。本方法一步合成手性噁唑啉,经X-衍射,1HNMR,IR,MS表征,其作为催化剂在苯甲醛的腈硅化反应及Baylis-Hillman反应中表现一定的催化活性。四、附图说明图1是化合物(I)的X-单晶衍射图。五、具体实施方式(一)化合物(I)的制备1、中间体1a 2-[(4R)-4,5-二氢化-4-(1′,1′-二甲基乙基)-2-噁唑啉基]苯酚的制备:在100mL两口瓶中,无水无氧条件下,加入无水ZnCl22.1g(15.4mmol),40mL氯苯,3-氰基苯酚3.8g(5.6mmol),L-亮氨醇8.7g,升温回流反应24h,停止反应,减压以除去溶剂,将剩余物加水溶解,并用CHCl3(30mL×2)萃取,有机相用无水硫酸钠干燥,旋转除去溶剂,将粗产品用石油醚/二氯甲烷(4∶1)柱层析,自然挥发得晶体,产率58%;[a]30D=-19.34°(c=0.362,CH2Cl2);1HNMR(500MHz,CDCl3,27℃),δ(ppm)=7.43(s,1H),7.34(d,J=7.5Hz,1H),7.19(t,J=0.5Hz,2H),6.94(d,J=8Hz,1H),4.49(t,1H),4.32(t,lH),4.00(t,J=0.5Hz,1H),1.67~1.76(m,2H),1.34~1.37(m,1H),0.89~0.92(m,6H)。13CNMR(125MHz,CDCl3,27℃)164.61,156.84,129.75,119.93,119.47,115.33,73.34,64.41,45.35,25.42,23.01,22.60.IR(KBr):3059,2961,2920,2907,2869,2846,2811,2690,2482,1643,1615,1584,1535,1492,1449,1368,1347,1330,1292,1219,1209,1167,1147,1135,1096,1065,1008,998,970,941,890,864,794,739,717,682,569,519;HRMS(EI):m/z(%):calcd for C13H17NO2:219.1259;found:219.1253.(二)腈硅化反应应用2-苯基-2-(三甲硅氧基)乙腈的制备
0.20mmol化合物I,苯甲醛0.1mL,TMSCN 0.3ml(3.3mmol)相继在20~30℃下加入,6h后,加入水淬灭经柱层后(石油醚/二氯甲烷:5/1),得无色油状液体,转化率:45%,1HNMR(300MHz,CDCl3)7.56-7.59(m,0.9Hz,2H),7.31-7.34(m,3H),5.43(s,1H),0.16(s,9H).13CNMR(75MHz,CDCl3)136.1,128.8(x2),126.2(x2),119.1,63.5,-0.39(x3).(三)Baylis-Hillmmn反应应用Baylis-Hillman反应早在1972年就已在一篇德国专利中有报道,指的是一类在合适的催化剂(如叔胺)的作用下由活化烯的α-位对sp2型缺电子试剂(如醛、酮、亚胺等)的亲核加成-消除反应,总的反应式可表示如下:
此反应具有选择性(化学的、区域的、立体的)、经济性,反应条件温和、产物具有多个可进一步转化的官能团(如醛与丙烯酸酯反应,可同时生成酯基、烯基以及羟基等官能团),且反应原料廉价易得,可应用于许多医药中间体和天然产物的合成。因此,从理论上讲,无论在实验室的有机合成还是在化学工业中,Baylis-Hil lman反应具有很广阔的应用前景。Baylis-Hillman反应机理是一个由叔胺、活化烯和亲电试剂共同参与的加成消除-反应历程。首先,叔胺与活化烯发生Michael型的亲核加成(1,4-加成),生成一个两性离子烯醇盐1,然后与亲电试剂发生Aldol缩合,生成
盐2,随后发生质子转移,产生两性烯醇盐3,3消去叔胺后得到产物.Baylis-Hillman反应机理如下:
2-(羟基-苯基-甲基)-丙烯酸甲酯的制备
在25mL的烧瓶中相继加入0.20mmol化合物I,苯甲醛0.1mL,丙烯酸甲酯0.5mL及2mLTHF,10天后,加入水淬灭,得无色油状液体,用1HNMR检测,转化率:20%。



企业营业执照
专利注册证原件
身份证
个体户营业执照
身份证
专利注册证原件
专利代理委托书
转让申请书
转让协议
手续合格通知书
专利证书
专利利登记簿副本





提交